Tóm tắt
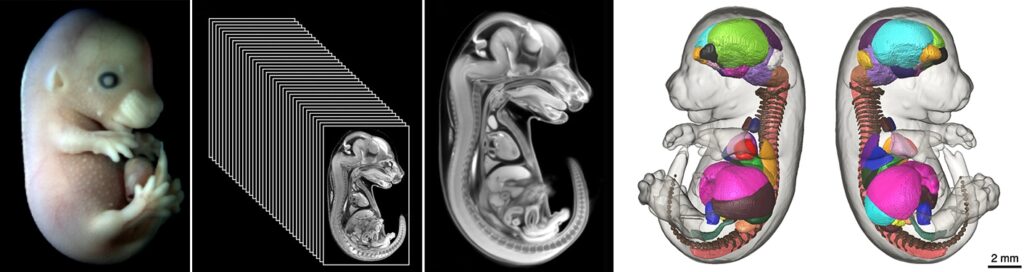
Kỹ thuật tạo ảnh hiển vi siêu phân giải (HREM) là một kỹ thuật phân tích 3D dựa trên các tập dữ liệu khối bao gồm các hình ảnh kỹ thuật số liên tiếp thu được từ bề mặt khối của phôi hoặc mô vùi nhựa methacrylate khi chúng được cắt lát vật lý. Vì hình ảnh được chụp từ mặt của khối nhựa (trong đó mẫu sinh học đã được vùi) chứ không phải từ các phần được gắn lam kính, nên bộ này vốn đã hoàn chỉnh, căn chỉnh và không gấp. HREM sử dụng huỳnh quang của eosin để cung cấp hình thái học. Mặc dù kỹ thuật này dựa trên hình ảnh hiển vi, nhưng chúng có độ phân giải cao và gần với chất lượng mô học.
Nguyên mẫu HREM được phát triển bởi trung tâm hình ảnh IGBMC và dịch vụ phôi học/giải phẫu bệnh học ICS (Illkirch, Pháp) bao gồm máy cắt lát tiêu bản quay HistoCore NANOCUT R của Leica Biosystems. Các khối đã được kiểm tra khả năng tái tạo độ dày lát cắt, chất lượng (đặc biệt là bề mặt khối) và quan trọng hơn là tái định vị khối ở chế độ 3D. Leica đã chứng minh rằng tất cả các thông số được thử nghiệm đều phù hợp với mục tiêu. Thật vậy, tính đều đặn của việc cắt lát là hiệu quả, bề mặt của khối sau khi cắt lát rất mịn và cuối cùng việc định vị lại khối có độ chính xác cao cho phép tái tạo mẫu 3D ngay lập tức mà không yêu cầu bước sắp xếp lại sau thu nhận.
Giới thiệu
Phân tích mô học của các mẫu sinh học đại diện cho tiêu chuẩn về độ phân giải, độ tương phản hình ảnh và độ nhạy để mô tả các khiếm khuyết về hình thái. Mặc dù tốn nhiều công sức và thời gian nhưng kỹ thuật này vẫn được áp dụng cho rất nhiều phân tích yêu cầu mô tả cấu trúc. Trong những thập kỷ qua, đã có sự phát triển của các công cụ hình ảnh tiên tiến để khám phá thông tin về cấu trúc và chức năng mới và hình ảnh đã cách mạng hóa nghiên cứu y sinh.
Việc áp dụng các kỹ thuật hình ảnh mới là các yêu cầu cụ thể và đa dạng của từng nhóm nghiên cứu. Ví dụ, trong lĩnh vực kiểu hình phôi, sự hình thành hình thái bất thường của các cấu trúc phát triển phức tạp trong phôi đang phát triển có thể khó hình dung bằng cách kiểm tra bên ngoài hoặc các phần 2D của phôi. Do đó, khả năng ghi lại hình ảnh kỹ thuật số ba chiều (3D) của các đột biến ở các giai đoạn phát triển khác nhau bằng cách sử dụng các công nghệ thông lượng từ trung bình đến cao sẽ làm tăng thêm giá trị cho thông tin do mô học cung cấp. Nó cho phép tự động phát hiện một số khiếm khuyết bằng cách so sánh với các tiêu chuẩn tự nhiên cũng như định lượng các thay đổi về hình thái. Bên cạnh lĩnh vực phôi học, việc kiểm tra hình dạng cơ quan của mô hình trưởng thành bằng 3D có thể thuận lợi vì kiểu hình có thể dễ phát hiện hơn so với các phần mô học 2 chiều, đặc biệt đối với các nhà nghiên cứu ít được đào tạo về giải phẫu.
HREM là một công cụ hiệu quả và mạnh mẽ để đánh giá các bất thường về cấu trúc trong phôi hoặc các cơ quan ngoài cơ thể. Về cơ bản, ‘mô học 3D’, một loạt các hình ảnh 2D liên tiếp của bề mặt khối mẫu, được ghi lại trong quá trình phân chia mô học của các mô cố định và mô vùi, cung cấp thông tin cấu trúc ở độ phân giải cao với các chi tiết gần giống với những thông tin thu được thông thường bằng cách sử dụng phân tích mô học. Dữ liệu HREM có thể được phân tích dưới dạng chồng hình ảnh 2D hoặc bằng cách hiển thị 3D và chúng có thể biểu hiện những thay đổi về hình thái mà không thể phát hiện bằng các kỹ thuật có độ phân giải thấp hơn như micro-CT hoặc MRI. Độ phân giải voxel của mô hình 3D chỉ bị giới hạn bởi độ dày của các phần được loại bỏ liên tiếp khỏi bề mặt khối. Trong thực tế, độ phân giải không gian 1µm là tiêu chuẩn.
Độ chính xác của việc căn chỉnh hình ảnh phụ thuộc rất nhiều vào việc mặt khối quay trở lại chính xác cùng vị trí để chụp ảnh sau mỗi chu kỳ phần. Thông số kỹ thuật này không phải là tiêu chuẩn cho máy cắt lát tiêu bản quay, cần phải sửa đổi để đảm bảo khả năng này. Một số máy cắt lát tiêu bản đã được thiết kế để có các vị trí dừng chính xác phù hợp để chụp ảnh (ví dụ: Leica SM2500), nhưng chúng không còn được thương mại hóa nữa. Gần đây, Leica Biosystems đã phát triển một máy cắt lát tiêu bản quay mới HistoCore NANOCUT R có thể kết hợp với hệ thống quang học và máy ảnh.
Quy trình thử nghiệm HREM
Nguyên tắc
Việc tạo kiểu hình phôi hoặc cơ quan của chuột bằng HREM yêu cầu mẫu phải được vùi vào nhựa. Các mẫu được rửa dần dần trong ethanol, trước khi được vùi vào nhựa JB4 để tạo ra khối phù hợp để cắt. Để tạo độ tương phản, nhựa vùi được hoàn thiện bằng Eosin B (phát huỳnh quang khi trộn trong JB4) và Acridine Orange (hấp thụ tín hiệu Eosin và tạo độ tương phản). Nhuộm eosin được biết đến nhiều từ mô học và Acridine Orange có ái lực mạnh với nhân, dẫn đến độ tương phản rất giống với chụp màu xám của nhuộm Hematoxylin & Eosin.
Mẫu vùi được Leica Biosystems đặt trên máy cắt lát tiêu bản của HREM HistoCore NANOCUT R và được chiếu sáng bằng ánh sáng xanh (phạm vi 450-500 nm) để thu được hình ảnh, sau đó một lát cắt được cắt ra khỏi khối để loại bỏ vật chất và quá trình này được lặp lại. Vì nồng độ Eosin trong nhựa rất cao, ánh sáng kích thích được hấp thụ trong phạm vi micromet từ bề mặt khối. Hiệu ứng này cho phép bạn coi các hình ảnh thu được từ HREM là dữ liệu bề mặt (dữ liệu được thu thập sẽ bị giới hạn ở độ sâu dưới 1µm và do đó sẽ không bao giờ vượt quá độ dày của phần ≥ 1µm). Độ dày của các phần sẽ được điều chỉnh theo kích thước pixel của hình ảnh để thu được các điểm ảnh ba chiều đẳng hướng (cùng kích thước theo kích thước x, y, z).
Kết quả là một loạt hình ảnh được chụp trên mẫu có thể được sử dụng để tái tạo lại dữ liệu hình ảnh ở dạng 3D, cho phép bạn kiểm tra một lát cắt theo bất kỳ hướng nào mà không làm giảm chất lượng.
Lưu ý rằng quá trình xử lý HREM mang tính phá hủy, mẫu được cắt thành nhiều phần và do đó, một mẫu chỉ có thể được chụp ảnh một lần. Điều này khiến cho việc thiết lập mẫu ban đầu trở nên quan trọng để có được hình ảnh tối ưu phục vụ phân tích mẫu tốt nhất.
Nguyên vật liệu
- Vật liệu sinh học: Phôi hoặc bào thai chuột, các mảnh mô trưởng thành không lớn hơn 20 mm.
- Chất cố định Bouin
- Bộ vùi nhựa JB-4 (Polysciences, Inc.)
- Eosin B (Sigma-Aldrich)
- Acridine Orange (Sigma-Aldrich)
- Ethanol 100% và loạt 70%, 80%, 90%, 95% trong H2O
- Khuôn polyetylen
- Dao cắt cacbua vonfram TC-65 (Leica Biosystems)
Vùi mẫu
- Cố định mẫu bằng chất cố định Bouin
- Rửa trong dung dịch etanol đã được phân loại: 70%, 80%, 90%, 95%, 100%
- Chuẩn bị hỗn hợp nhựa JB4 chứa Acridine orange và eosin.
- Ủ trong hỗn hợp nhựa/etanol (1:1)
- Ủ trong hỗn hợp nhựa nguyên chất
- Chuẩn bị nhựa JB4 mới hoạt hóa
- Polyme hóa đệm ở đáy khuôn
- Đặt mẫu lên đệm vào khuôn chứa nhựa hoạt tính và polyme hóa nhựa ở nhiệt độ 4°C qua đêm. Nhựa được phủ một lớp dầu khoáng để tránh tiếp xúc với không khí.
- Làm cứng thêm khối ở 95°C
Xác định vị trí mẫu trong khối bằng cách sử dụng nguồn sáng xiên và cắt phần nhựa không chứa mẫu thử (sẽ cho phép điều chỉnh ở độ phóng đại tốt hơn)
Tiêu chuẩn cắt lát
- Gắn khối lên Máy cắt lát tiêu bản quay HistoCore NANOCUT R của Leica Biosystems
- Sử dụng chế độ 3D của microtome
- Cắt khối cho đến khi bắt đầu mẫu vật
- Điều chỉnh tiêu điểm
- Bắt đầu phân chia và chụp ảnh tự động. Các mô-đun phần mềm được điều chỉnh đặc biệt (Phần mềm MetaMorph® hoặc phần mềm tự chế có sẵn theo yêu cầu) sẽ cho phép đồng bộ hóa quá trình cắt và chụp ảnh.
- Các phần có thể được thực hiện từ 2µm đến 7µm. Ví dụ, phôi ở giai đoạn E15.5 được cắt ở kích thước 7µm.
- Để xử lý dữ liệu, hãy tối ưu hóa ánh xạ thang độ xám như mong muốn; chia tỷ lệ dữ liệu và/hoặc mẫu phụ phù hợp với phần mềm kết xuất 3D.
Kết quả
A. Thiết bị nguyên mẫu cho hình ảnh ngoại soi
Nguyên mẫu HREM bao gồm một camera SCMOS, bộ lọc huỳnh quang GFP, nguồn sáng LED, thiết bị quang học (kính hiển vi), gương, giá đỡ dao và mẫu được gắn trên máy cắt lát tiêu bản quay HistoCore NANOCUT của Leica Biosystems.

B. Chất lượng và tính đều đặn của việc cắt lát
Ngay cả khi chỉ có hình ảnh được chụp từ mặt của khối nhựa, các phần được cắt lát có thể hiển thị trên ảnh. Các khối nhựa được cắt theo các bước từ 2µm đến 7µm. Dao cắt cacbua vonfram TC-65 (Leica Biosystems) đã được sử dụng để cắt các khối. Trên ba khối được cắt bằng HistoCore NANOCUT R của Leica Biosystems, bề mặt của khối rất hoàn hảo và không quan sát thấy vật phẩm nào (hình 3).
C. Tái tạo 3D
Sự cải tiến của máy cắt lát tiêu bản quay HistoCore NANOCUT R của Leica Biosystems nằm ở chế độ tùy chọn 3D. Điều này có nghĩa là so với các máy cắt lát tiêu bản khác, nó đã được sửa đổi để cho phép giá đỡ khối có thể tái tạo ở một “vị trí chụp ảnh” sau mỗi lần cắt. Vị trí càng chính xác thì việc căn chỉnh càng chính xác và thu được kết quả tái tạo 3D tốt nhất. Dữ liệu HREM có thể được phân tích dưới dạng hình ảnh 2D hoặc bằng cách hiển thị 3D bằng phần mềm thích hợp. Nhờ căn chỉnh hình ảnh và thu được các pixel đẳng hướng, có thể thu được các chế độ xem trực giao và xiên của mẫu mô từ dữ liệu HREM. Với các khối đã được thử nghiệm, “vị trí ảnh” đã thu được một cách hoàn hảo bằng chế độ 3D của HistoCore NANOCUT R. Quá trình tái tạo 3D tốt đến mức không cần thiết phải tổ chức lại từng bước sau khi thu được.
Thảo luận
Sự phát triển của máy cắt lát tiêu bản quay HistoCore NANOCUT R của Leica Biosystems với tùy chọn 3D đang rất được quan tâm cho các phòng thí nghiệm phát triển triển công nghệ HREM. Việc thực hiện các phần tự động bằng HistoCore NANOCUT R giúp tăng khả năng tái tạo các thông số chính như bề mặt cắt và định vị chính xác của khối giúp căn chỉnh hoàn hảo các phần và nâng cao chất lượng tái tạo 3D.
Hình ảnh kỹ thuật số HREM mang lại một số lợi thế so với các phần mô học thông thường. Thứ nhất, chúng không hiển thị các biến dạng do quá trình cắt, xử lý phần hoặc lắp đặt gây ra. Hơn nữa, một loạt hàng nghìn hình ảnh được tạo ra trong vòng vài giờ theo cách tự động, trái ngược với nhiều tuần để tạo ra một loạt hình ảnh kỹ thuật số được sắp xếp lại chính xác ít nhiều từ hàng nghìn phần mô học. Dữ liệu khối lượng HREM có thể được phân tích ngay lập tức bằng các công cụ phân chia lại ảo trực giao và xiên và phần mềm thích hợp.
HREM đã được chứng minh là một công cụ tối ưu trong nhiều lĩnh vực nghiên cứu. Ngoài việc sử dụng HREM ngày càng tăng để hình dung phôi nhằm sàng lọc kiểu hình của phôi chuột E14.5/E15.5 gây chết trước khi sinh được sản xuất cho International Mouse Phenotyping Consortium (IMPC), gần đây đã xuất hiện cũng được sử dụng để hiển thị các mẫu mô của các sinh vật mô hình y sinh trưởng thành, sinh thiết da và các vật liệu sinh học được sử dụng trong y học hiện đại. Các kết quả rất đáng khích lệ đưa chúng tôi đến kết luận rằng HREM có tiềm năng trở thành một công cụ có giá trị trong nhiều lĩnh vực nghiên cứu tiền lâm sàng và tiền lâm sàng trong thập kỷ tới.
Do đó, HREM cung cấp thông tin chất lượng cao và chi phí thấp bằng cách sử dụng các thiết bị phòng thí nghiệm sẵn có, điều này đặc biệt quan trọng đối với các nhà nghiên cứu.
Minh Khang là nhà phân phối và nhập khẩu trực tiếp các sản phẩm máy cắt lát tiêu bản quay hãng Leica Biosytems.


 EN
EN