Chất cố định mô
Cũng như formaldehyde và glutaraldehyde, một số thuốc thử khác đã được sử dụng để cố định mô, đôi khi ở dạng dung dịch đơn giản nhưng thường kết hợp với các tác nhân khác ở dạng hợp chất cố định.
Acrolein
Acrolein hoặc acrylic aldehyde (H 2 C=CH.CHO) phản ứng với các đại phân tử theo kiểu tương tự như formaldehyde tạo thành các liên kết chéo thuận nghịch. Nó đã được chứng minh là tạo ra nhiều liên kết chéo hơn formaldehyde. Acrolein phản ứng với axit béo thông qua liên kết đôi của nó. Mặc dù acrolein thâm nhập vào mô nhanh chóng và có tính phản ứng cực cao nhưng nó vẫn chưa được sử dụng phổ biến vì khó sử dụng (chất gây chảy nước mắt), không ổn định ở pH kiềm và dễ dàng tạo thành polyme. Nó chủ yếu được sử dụng cho mô hóa học enzyme và để cố định nguyên liệu thực vật. Sau khi cố định các nhóm carbonyl dư trong mô sẽ gây ra vết nền bằng các kỹ thuật như PAS.
Glyoxal
Glyoxal hoặc diformyl (CHO.CHO) là một aldehyd hai chức năng phản ứng theo cách tương tự với formaldehyde tạo ra dạng hình thái tương tự. Mỗi nhóm aldehyd đều có khả năng phản ứng và có thể hình thành các liên kết chéo. Glyoxal là thành phần chính trong một số chất cố định độc quyền, đặc biệt áp dụng cho việc cố định bằng lò gia nhiệt cũng như cho các công việc thường ngày. Nó thường được gọi là “chất thay thế formalin” vì nó được khẳng định là ít nguy hiểm hơn khi sử dụng so với formaldehyde vì nó hầu như không tạo ra hơi ở nhiệt độ phòng có áp suất hơi cực thấp. Mặc dù nó là một chất gây kích ứng và có khả năng gây mẫn cảm khi tiếp xúc với da nhưng hiện tại nó không được phân loại là chất gây ung thư, mặc dù có cảnh báo về tác dụng gây đột biến tiềm tàng của nó. Nó phản ứng với các chất cộng tạo thành DNA một cách không ổn định và có thể đảo ngược. Nó được cho là có khả năng phân hủy sinh học nên việc xử lý sẽ dễ dàng hơn so với formalin.
Osmi tetroxit
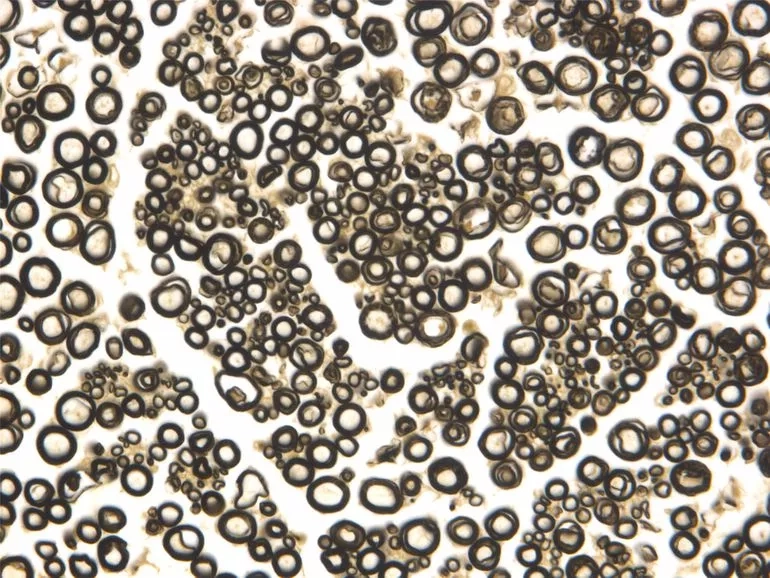
Osmium tetroxide (OsO4 ) là một chất rắn kết tinh có độc tính cao, dễ bay hơi, được cung cấp dưới dạng ống kín. Do tính dễ bay hơi của nó, nó phải được xử lý hết sức cẩn thận trong tủ hút vì nó sẽ dễ dàng cố định kết mạc của mắt và niêm mạc mũi. Nó hòa tan trong dung môi phân cực và không phân cực và phản ứng với chuỗi bên của protein tạo thành liên kết chéo. Các phản ứng cố định quan trọng nhất của osmium tetroxide là những phản ứng liên quan đến liên kết không bão hòa của lipid và phospholipid vì đây là một trong số ít chất cố định giúp ổn định lipid. Trong quá trình cố định, osmium tetroxide bị khử thành các oxit thấp hơn, có màu đen và không hòa tan và chúng lắng đọng trong các mô, đặc biệt là trên màng. Bởi vì osmium là một kim loại nặng nên nó làm tán xạ các electron và do đó làm tăng mật độ electron cho hình ảnh kính hiển vi điện tử. Nó cũng có thể được sử dụng như một chất nhuộm tổng thể để kiểm tra lipid (đặc biệt là các sợi thần kinh có myelin) ở cấp độ kính hiển vi ánh sáng. Nói chung, nó được sử dụng ở mức khoảng 1% w/v như chất cố định thứ cấp chuyên dụng cho kính hiển vi điện tử và cho các chế phẩm sợi thần kinh bị đứt.
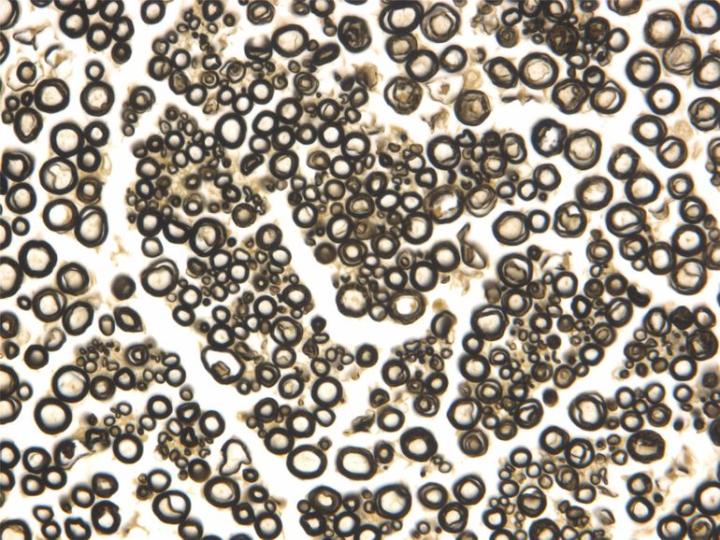
Carbodiimide
Carbodiimide (RN=C=NR’) là những hợp chất rất dễ phản ứng sẽ phản ứng với nhiều nhóm chức. Các phản ứng có thể được tăng cường hoặc ngăn chặn có chọn lọc bằng cách chọn một loại carbodiimide, pH, nhiệt độ hoặc chất xúc tác cụ thể. Bởi vì các liên kết peptide có thể hình thành do phản ứng cố định và sau đó chúng có thể bị phá vỡ một cách có chọn lọc bằng cách sử dụng protease, nhóm hợp chất này được cho là có tiềm năng sử dụng trong hóa mô miễn dịch cũng như mô học thông thường. Carbodiimides đã được sử dụng để điều chế các chất gây miễn dịch.
Các tác nhân liên kết chéo khác
Diimidoesters là các hợp chất hòa tan trong nước, liên kết chéo các nhóm protein protein và đã được sử dụng cho kính hiển vi điện tử và hóa mô miễn dịch. Cloro-s-triazide (cyanuric chloride ) đã được sử dụng làm chất nhầy tuyến nước bọt và miễn dịch huỳnh quang. Diisocyanate đã được sử dụng để gắn thẻ huỳnh quang vào protein, trong khi Diethylpyrocarbonate (DPC) phản ứng với dư lượng tryptophan và được sử dụng làm chất cố định pha hơi cho mô đông khô. Trong dung dịch đệm thích hợp, nó được đề xuất dùng làm chất cố định cho các mẫu vật nhỏ. Maleimide dường như hình thành một số liên kết chéo với protein và Benzoquinone phản ứng với các amin, axit amin và peptide và đã được sử dụng để cố định peptide trong các mô nội tiết cho chất hóa mô miễn dịch.
Thủy ngân clorua
Thủy ngân clorua (HgCl2 ) là một trong những thuốc thử đầu tiên được sử dụng để cố định mô. Trong tài liệu cũ, nó được gọi là “chất ăn mòn thăng hoa”, một cái tên thích hợp vì nó là một chất hóa học ăn mòn phản ứng với các kim loại bao gồm cả thép không gỉ của dụng cụ phẫu tích. Mặc dù cơ chế cố định mô của nó chưa được hiểu đầy đủ nhưng nó được biết là phản ứng với các amin, amit, axit amin và các nhóm sulphydryl, chất sau nổi bật trong phản ứng với cysteine, nơi nó được cho là tạo ra liên kết chéo. Nó là một chất đông tụ protein mạnh, khiến mô ở trạng thái tạo ra màu nhuộm mạnh bằng thuốc nhuộm axit. Nó phản ứng với dư lượng photphat của axit nucleic và cố định nucleoprotein một cách hiệu quả. Vì lý do này mà nó là thành phần chính trong các chất cố định có công thức như B-5 và Helly’s, các chất cố định được khuyên dùng khi cần bảo quản hạt nhân chất lượng cao (ví dụ trephin tủy xương).
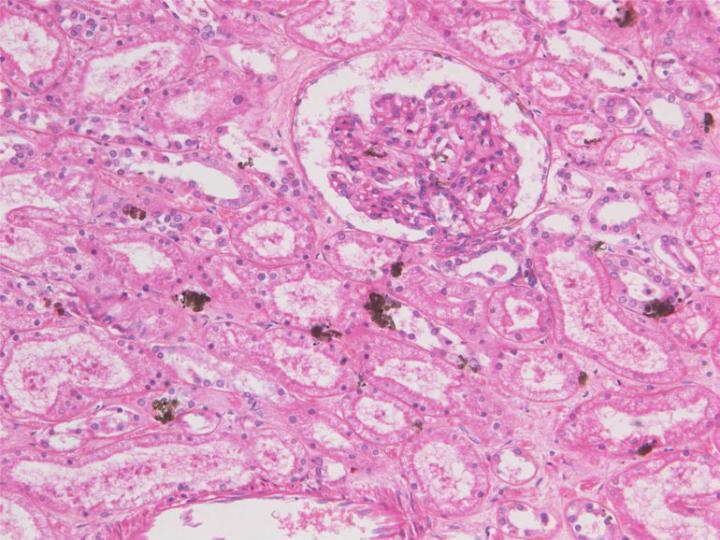
Có một số nhược điểm khi sử dụng chất cố định có chứa clorua thủy ngân. Ngoài tính chất ăn mòn của thủy ngân clorua, thủy ngân còn có độc tính cao, có thể hấp thụ qua da và là chất độc tích lũy. Ở hầu hết các nước đều có những quy định nghiêm ngặt về việc thải bỏ thủy ngân và các hợp chất có chứa thủy ngân. Trong quá trình cố định bằng chất cố định có chứa thủy ngân clorua, một sắc tố giả màu xanh lục kết tinh hoặc vô định hình của thủy ngân được lắng đọng ngẫu nhiên trong các mô. Xử lý mẫu bằng iốt (iốt Lugol) trong quá trình xử lý hoặc cắt lát trước khi nhuộm sẽ tạo ra iodua thủy ngân có thể được rửa sạch khỏi mô. Việc xử lý tiếp theo bằng natri thiosulphate sẽ loại bỏ lượng iốt còn sót lại. Các chất cố định gốc thủy ngân clorua có xu hướng thẩm thấu kém và nếu quá trình cố định kéo dài, các mô sẽ trở nên rất cứng và dễ bị co rút trong quá trình xử lý.
Trong những năm gần đây, một số muối kim loại đã được sử dụng làm chất thay thế cho clorua thủy ngân bao gồm muối kẽm và bari. Kẽm clorua và kẽm sunfat được xem là phù hợp và hiện nay có nhiều chất thay thế B-5 độc quyền.
Muối kẽm
Kẽm sunfat (ZnSO4 ) và kẽm clorua (ZnCl2 ) được sử dụng thay thế cho clorua thủy ngân trong một số chất cố định có công thức và độc quyền, sunfat phổ biến hơn vì nó có khả năng ăn mòn ít hơn clorua đã được báo cáo là gây ra vấn đề trong bộ xử lý mô. Muối được thêm vào dung dịch formalin 10% (dung dịch nước hoặc cồn, đệm hoặc không đệm), ở nồng độ khoảng 1%, nhưng đã có một số vấn đề được báo cáo về việc kết tủa kẽm hoặc muối đệm trong quá trình chuẩn bị. Muối kẽm sẽ phản ứng với nhiều nhóm cuối cùng của mô bao gồm amino, carboxyl và sulphydryl, tạo thành các sản phẩm phản ứng thuận nghịch, một số trong đó có thể được loại bỏ bằng nước rửa citrate hoặc EDTA. Kẽm được cho là có khả năng tăng cường khả năng cố định và nhuộm màu, đặc biệt là ở hạt nhân, theo cách tương tự như clorua thủy ngân. Nó được cho là có lợi thế trong việc duy trì khả năng phản ứng miễn dịch khi so sánh với formalin đơn thuần, loại bỏ nhu cầu thu hồi kháng nguyên đối với một số epitope. Muối kẽm ít độc hơn nhiều so với muối thủy ngân và việc thải bỏ dung dịch kẽm sẽ không gây ra vấn đề gì
Axit picric
Axit picric hay trinitro phenol (C6H2(NO2)3OH) là chất kết tinh màu vàng sáng, phải bảo quản ướt bằng nước để tránh nguy cơ nổ do va đập hoặc đun nóng chất khô. Nó nên được giữ trong một hộp kín và thường xuyên kiểm tra xem nó có bị ẩm không. Có thể thêm nước cất nếu nước cất bị khô. Để cố định, nó luôn được sử dụng kết hợp với các tác nhân khác. Ngoài việc là một thành phần của chất cố định, axit picric còn được sử dụng làm thuốc nhuộm axit trong một số vết bẩn (ví dụ: trong dung dịch nhuộm cơ của Van Gieson). Nó tạo ra màu vàng cho các mô trong quá trình cố định và do tính chất axit nên axit picric dư nên được rửa khỏi mô bằng ethanol 70% trước khi xử lý. Nếu axit picric còn sót lại trong khối mô sau khi xử lý thì đặc tính nhuộm màu của mô sẽ bị ảnh hưởng và sẽ xấu đi theo thời gian.
Axit picric là chất cố định đông tụ, làm thay đổi điện tích trên chuỗi bên có thể ion hóa của protein và phá vỡ liên kết tĩnh điện và hydro. Nó tạo thành muối (picrates) với các nhóm protein cơ bản gây đông máu. Nó dường như không cố định lipid hoặc hầu hết carbohydrate nhưng được khuyên dùng như một thành phần trong chất cố định dùng để bảo quản glycogen. Axit picric có thể thủy phân axit nucleic nên cần tránh sử dụng nếu muốn chứng minh DNA hoặc RNA. Axit picric sẽ hòa tan cặn canxi nhỏ trong mẫu vật. Một lượng co rút đáng kể xảy ra trong quá trình xử lý các mô được cố định trong thuốc thử chứa axit picric.
Kali dicromat
Kali dicromat (K2Cr2O7 ) hoạt động như một chất không đông tụ trừ khi nó được sử dụng ở pH < 3,4 – 3,8, nơi nó phản ứng như axit cromic, ở dạng chất đông tụ. Nó là thành phần của một số chất cố định phức hợp. Các phản ứng cố định được cho là liên quan đến quá trình oxy hóa protein với sự tương tác của các ion cromat khử tạo thành một số liên kết ngang, mức độ được xác định bởi độ pH của chất cố định. Các ion crom được báo cáo là phản ứng với chuỗi bên carboxyl và hydroxyl của protein. Nó để lại các nhóm amino có sẵn và do đó thích nhuộm bằng thuốc nhuộm axit. Cromat sẽ phản ứng với các lipid không bão hòa khiến chúng không hòa tan, vì lý do này mà nó được coi là chất cố định tốt cho ty thể. Thông thường, khuyến cáo rằng các mô được cố định trong chất cố định có chứa cromat nên được rửa kỹ trong nước trước khi xử lý để tránh hình thành oxit phụ cromat không hòa tan do phản ứng của rượu xử lý và muối cromat. Theo truyền thống, chất cố định có chứa dicromat được sử dụng trong các phương pháp mô hóa học đối với các hạt “chromaffin” chứa amin của các mô nội tiết.
Ethanol và metanol
Ethanol (CH 3 CH 2 OH) và metanol (CH 3 OH) được coi là chất đông tụ làm biến tính protein. Chúng thay thế nước trong môi trường mô, phá vỡ liên kết kỵ nước và hydro, do đó làm lộ ra các nhóm kỵ nước bên trong của protein và làm thay đổi cấu trúc bậc ba cũng như khả năng hòa tan của chúng trong nước. Metanol có cấu trúc gần với nước hơn etanol nên etanol tương tác với vùng kỵ nước mạnh hơn metanol. Quá trình cố định bắt đầu ở nồng độ 50 – 60% đối với ethanol và >80% đối với metanol. Ethanol đôi khi được sử dụng để bảo quản glycogen nhưng sẽ gây biến dạng chi tiết hạt nhân và tế bào chất. Methane thường được sử dụng làm chất cố định cho màng máu và ethanol 95% được sử dụng làm chất cố định cho phết tế bào học nhưng cả hai loại rượu này thường được kết hợp với các thuốc thử khác khi được sử dụng làm chất cố định cho mẫu mô.
Aceton
Acetone (CH3COCH3) có tác dụng tương tự như rượu và đã được sử dụng làm chất cố định và khử nước để xử lý mô, đặc biệt là xử lý thủ công nhanh chóng các mẫu vật nhỏ. Nó được khuyến khích sử dụng rộng rãi để cố định như một phần của quá trình chứng minh mô hóa học của các enzym trong đó nó thường được sử dụng ở nhiệt độ lạnh (4°C). Nó là một dung môi lipid hiệu quả với tác dụng nhanh có thể làm cho các mô trở nên rất giòn. Bởi vì nó rất dễ bay hơi và dễ cháy nên thường không được sử dụng trong các máy xử lý mô tự động.
Không nên sử dụng Acetone trên một số bộ xử lý mô vì nó sẽ ảnh hưởng xấu đến các vòng đệm và các bộ phận khác của thiết bị.
Axit axetic
Axit axetic (CH3COOH) là chất đông tụ khi tác dụng với axit nucleic nhưng nhìn chung không cố định được protein. Nó được kết hợp trong các chất cố định hợp chất để giúp ngăn ngừa sự mất mát axit nucleic và do nó làm phồng collagen nên chống lại sự co rút do các thành phần khác như ethanol gây ra. Axit axetic thẩm thấu rất nhanh nhưng chất cố định có chứa nó sẽ làm tan hồng cầu.
Minh Khang là nhà phân phối và nhập khẩu trực tiếp các thiết bị Giải phẫu bệnh từ hãng Leica Biosystems.


 EN
EN